El Agua como Fluido Caloportador
La industria procesa grandes cantidades de energía en equipos e instalaciones en las que su principio básico de funcionamiento es mover energía, utilizando un fluido que como su nombre lo indica transporta calor (caloportador). El fluido caloportador más utilizado, sin dudas, es el agua, en los estados líquidos y vapor, aunque también está muy extendido el uso de productos inorgánicos como el amoniaco y otros orgánicos como los freones.
Lo que hoy comentaremos hace referencia exclusiva al agua y al vapor, aunque puede ser aplicable a cualquier fluido que realice el cambio de fase. La energía acumulada en el agua al suministrarle calor, por ejemplo, utilizando una caldera, y cedida en los puntos de utilización, es una de las formas más comunes para la transmisión de calor entre puntos distantes en la industria.
El agua es el fluido caloportador más utilizado gracias a:
- Facilidad de obtención
- Es económica
- Tiene un elevado calor especifico
- Elevado calor de vaporización
- Temperatura ajustable fácilmente ajustando su presión.
- No es tóxica ni supone riesgo de explosión o incendio.
Otros Fluidos caloportadores utilizados en la industria
- Aire
- Sales Fundidas
- Mercurio
- Sodio líquido
- Aceites térmicos
Conceptos a tener en cuenta en el estudio del Agua como caloportador
Cuando revisamos la bibliografía que hace referencia al agua en los sistemas energéticos, nos encontraremos con formas específicas de llamar cada estado. Ágamos un resumen:
1- El calor que acumula el agua al pasar de una temperatura inicial X hasta una temperatura cualquiera Y se denomina calor sensible a dicha temperatura.
2- Cuando el agua llega a 100 ºC y 1 atmosfera, se denomina líquido saturado. Es la región límite entre el líquido subenfriado y la mezcla líquido vapor. En ese punto se inicia el cambio de fase del líquido al vapor.
3- El calor absorbido por el agua una vez alcanzada la temperatura de vaporización, para cambiar su estado de líquido a vapor, se denomina calor latente, obteniéndose al final vapor saturado.
4- El líquido a una temperatura inferior a la de su punto de ebullición para una presión determinada recibe el nombre de líquido subenfriado.
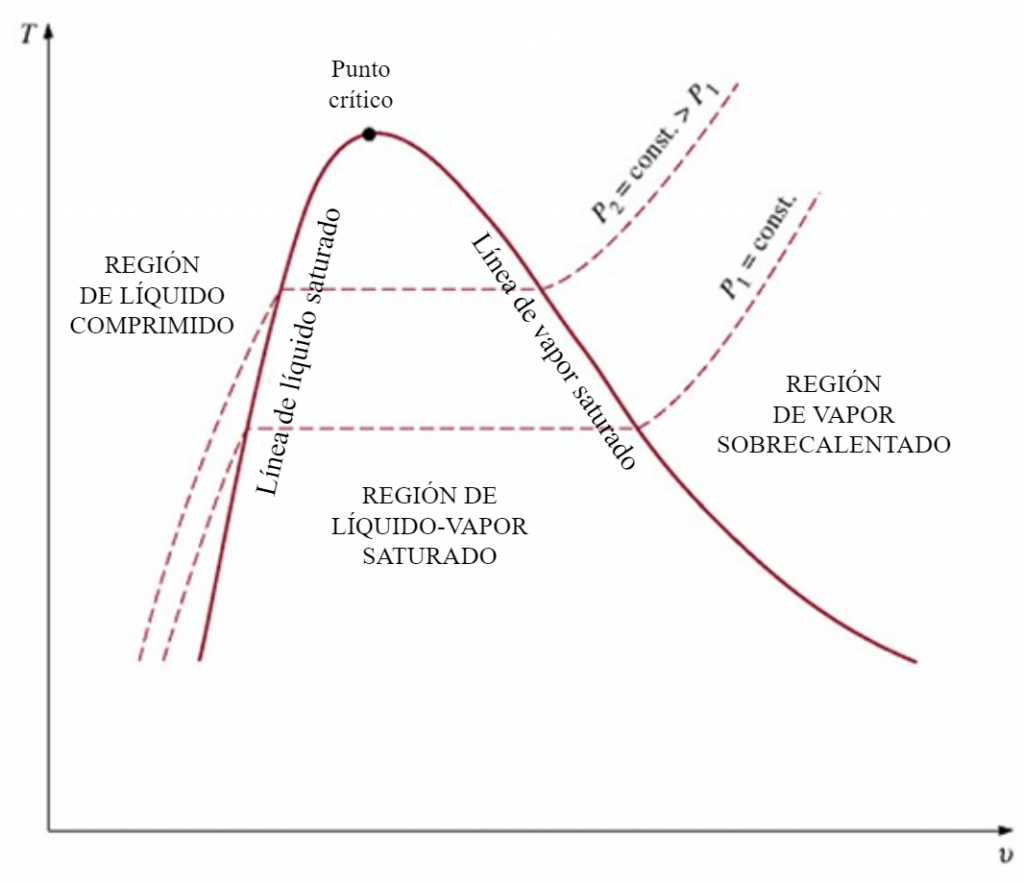
Se debe comprender que al someter a agua a un aumento de presión, la temperatura a la cual comienza su vaporización también crece. Esto sucede porque el aumento de presión hace que las moléculas de agua encuentren mayor dificultad para abandonar el líquido, lo que obliga a un aumento en la aportación de energía (temperatura) para romper las fuerzas de cohesión moleculares.
Vapor como caloportador
El vapor de agua puede ser utilizado como un caloportador, es decir, como un medio para transportar calor de un lugar a otro. Esto se logra mediante el uso de un intercambiador de calor, en el cual el vapor entra en contacto con un material que se encarga de transferir el calor.
Un ejemplo común de esto es en un sistema de calefacción central, donde el vapor es generado en una caldera y luego es enviado a través de tuberías hasta radiadores en diferentes puntos de la casa. El vapor entra en contacto con los radiadores y transfiere su calor al aire circundante, calentando así la casa.
También se utiliza en industrias para el procesamiento de alimentos, producción de energía eléctrica, procesos químicos y muchos otros. El vapor de agua es un caloportador eficiente debido a su gran capacidad de almacenamiento de calor y su capacidad de transportar calor a través de tuberías, lo que permite una distribución fácil y eficiente del calor en un sistema.
Si nos encontramos utilizando vapor saturado y este cede calor, debemos tener en cuenta que este lo hace cediendo calor latente. Cuando haya cedido todo el calor latente que posea cambiará su fase y se convertirá en líquido saturado. Cuando el vapor se condensa, siempre conlleva que este ceda su calor latente en la misma cantidad que se tuvo que aportar para su formación.
Volumen que ocupa un litro de agua al transformarse en vapor
El vapor, era con anterioridad una masa de agua con menor volumen, al aumentar la temperatura a una presión determina se convirtió en vapor. Este vapor, si tomamos como partida de ejemplo 1 kg de agua a presión atmosférica, ocupa el orden de 1700 veces más volumen que en su estado líquido inicial. La misma cantidad de vapor sometida a una presión de 20 kg/cm2 todavía ocuparía casi 100 veces más volumen que el kilogramo de agua líquida.

Estos volúmenes, sin duda considerables, se deben tener en cuenta para implementar un correcto dimensionamiento de las instalaciones. Deben existir purgadores de vapor bien seleccionados y dimensionados según las condiciones de trabajo. Si el condensado se llega a desplazar a la velocidad del vapor, sin dudas provocaría grandes daños en las instalaciones.







